Le silane est le composé de formule SiH4, analogue silicié du méthane.
Il donne son nom aux silanes, des composés chimiques de formule SinH2n+2 analogues siliciés des alcanes. D'une manière générale, les silanes sont plus réactifs que les alcanes correspondants. La réaction avec l'eau est très difficile dans l'eau pure, mais se trouve considérablement facilitée avec un acide fort ou simplement en présence de traces basiques.
En traitement de surface, on utilise des dérivés alkyl et alkoxy silanes, également appelés organosilanes et plus communément ‘silanes’. Cette dernière appellation, bien qu’erronée, est la plus courante et est donc acceptée dans le domaine du traitement de surface.
La formule générale des organosilanes est RnSi(OR)4-n où R peut être un alkyl, aryl ou un groupement organofonctionnel et OR (hydrolysable) peut être un metoxy, etoxy, acetoxy,…

Exemples :
- TEOS (tetraetoxysilane) : (CH3CH2O)4Si
- BTSE : (CH3CH2O)3-Si-(CH2)2-Si-(OCH2CH3)3
- APS : (CH3CH2O)3-Si-(CH2)3-NH2
Les couches de silanes sont issues de traitements de surface basés sur des produits sans chrome ou métaux lourds. Elles sont spécialement conçues pour le traitement de surface avant peinture, afin de remplacer les phosphatations au fer, au zinc et les chromatations.
Les couches de silanes augmentent les performances de protection contre la corrosion du support traité, avec ou sans peinture. Les applications potentielles peuvent être trouvées dans l'automobile,le coil coating et dans l’industrie en général.
Le fait de pouvoir appliquer les silanes sur de multiples matériaux est aussi très positif car il permet de réduire les frais de conception d’une nouvelle installation. Finalement, les températures de traitement relativement basses (température ambiante) évitent le chauffage et donc réduisent les dépenses énergétiques.
Principe du schéma réactionnel
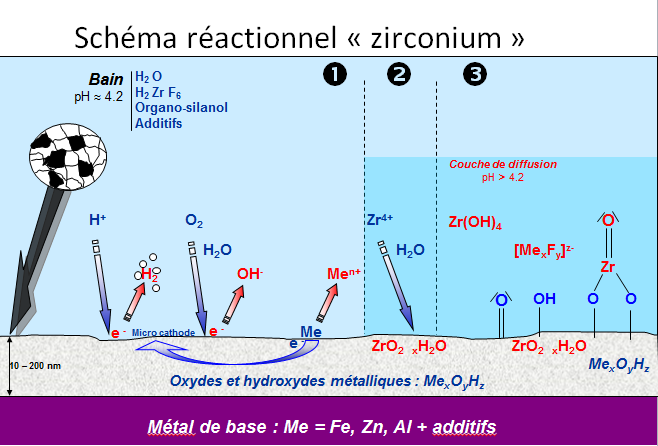
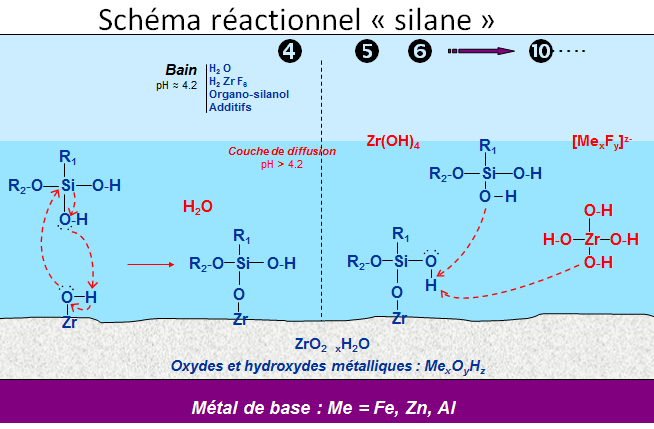
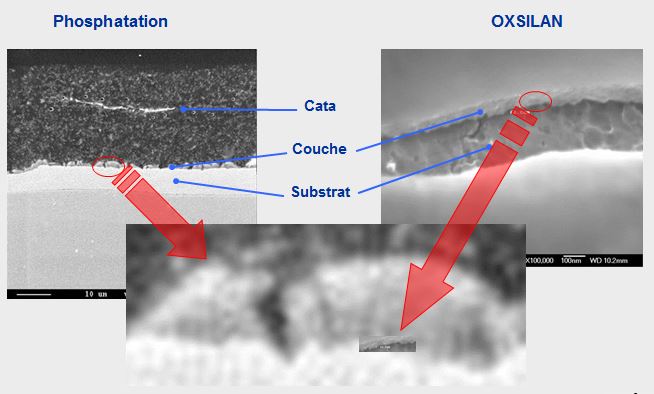
Couche formée

Les couches formées sont de l'ordre de 10 à 800 nm